Sugárterhelés
„A blog a TÁMOP 4.2.4.A/1-11-1-2012-0001 azonosító számú Nemzeti Kiválóság Program – Hazai hallgatói, illetve kutatói személyi támogatást biztosító rendszer kidolgozása és működtetése országos program című kiemelt projekt keretében valósul meg, az Európai Unió támogatásával, az Európai Szociális Alap társfinanszírozásával.”
2014. április 13., vasárnap
A Nemzeti Kiválóság Hírlevélben megjelent anyag
A Nemzeti Kiválóság Hírlevél márciusi számának 6. oldalán a blog által is megcélzott témában kifejtett kutatásaimról írnak. Az írás szabadon hozzáférhető itt:
http://www.nemzetikivalosag.hu/documents/10179/10351224/NKP_Hirlevel_2014-03_Marcius_FIN.pdf/a6aa509d-adcd-492f-84a0-26cf3ad6601c
2014. március 28., péntek
A sugárzás hatásának egy lehetséges modellezése. III. Rész: A légutakban kiülepedett radioaktív izotópok kölcsönhatása a sejtekkel
Jelen bejegyzésben
két biológiai végpontnak, nevezetesen a sejthalálnak és a sejttranszformációnak a
szimulációjáról lesz szó. Az előző két posztban láthattuk, hogy a rüvid felezési idejű radon leányelemek lokális légúti terhelése függ azok kiülepedési helyétől tisztulásától. A kiülepedett és még ki nem tisztult rövid felezési idejű alfa-bomló izotópok ha elbomlanak, akkor a kiülepedés helyéhez közeli sejteket alfa-találat érheti. E sejtekben energialeadás történik, melynek biológiai következményeit modellezhetjük. Ehhez ismernünk kell a bomlás során keletkező alfa-részecske kezdeti energiáját, a sejtekben egységnyi úthosszon leadott energiát, valamint a sejtszerkezetet. A rövid felezési idejű radon bomlástermékek közül a 218Po és a 214Po alfa-aktívak. Míg az előbbi egy 6 MeV-es, addig az utóbbi egy 7,69 MeV-es alfa-részecskét bocsát ki. A kibocsátás egyforma eséllyel történhet a tér bármely irányában, ezért a légutak falára kiülepedett alfa-bomló izotóp által kibocsátott alfa-részecske vagy behatol a szövetbe, vagy átrepül a légúton (a légút belsejében lévő levegőn) és a "túloldalon" csapódik be és lépik be a légúti hámsejtekbe. A levegőben leadott energia viszonylag kicsi a szövetben elnyelthez képest. A sejteken áthatoló alfa-részecske az energiáját nem egyenletesen adja le, hanem a Bragg-törvény szerint, vagyis minél mélyebben hatol be, annál több energiát képes leadni egységnyi úthosszon, mígnem energiája teljes elvesztésének közelében hirtelen lecsökken ezen érték.
A sejtekben a sugárzás hatására végbemenő folyamatok nagymértékben függnek attól, hogy mekkora energia (és dózis, ami energia/tömeg) nyelődött el bennük. Ez attól függ, hogy az eltalált sejtet mekkora úthosszon (húrhossz) metszi az alfa-nyom (alfa-részecske pályája) és mekkora ott az egységnyi úthosszra jutó leadott energia. Ennek kiszámításához modellezhetjük a tüdő hámszövetének sejteloszlását. Az irodalmi adatok alapján a sejtstruktúrát 3D számítógépes módszerekkel rekonstruálhatjuk. Két különböző típusú sugárérzékeny sejttípus eloszlását az alábbi ábrán láthatjuk. E sejtek a jobb oldalon lévő hámrétegben helyezkednek el, mely közvetlenül a bal oldalon megjelenített légút falához tapad.
Látható, hogy a sejthalál esélye a dózissal nő, illetve az is, hogy az inhomogén kiülepedés forró területén (elágazás csúcsa, ahol sok részecske kiülepszik) a sejthalál valószínűsége erősen megnő. Ugyanezen az ábrán szépen látszik a tisztulás kárcsökkentő szerepe is.
Ha most a sejttranszformációt vesszük alapul, akkor a neki megfelelő grafikon a következő lesz:
Az ábrán az látható, hogy a transzformáció esélye miként nő, ugyancsak az eltelt idő függvényében, a fenti három esetben (egyenletes kiülepedés, inhomogén depozíció tisztulás nélkül és egyenletlen kiülepedés tisztulással) ha a radon aktivitás koncentrációja 50 Bq/m3. Láthatjuk, hogy a transzformáció valószínűsége is nő a dózissal (besugárzási idővel), de az értéke sokkal kisebb, mint a sejthalálé. Megjegyzendő, hogy a fenti két ábrán csak a direkt hatások (csak az a sejt károsodik, amelyik a dózist kapja) vannak feltüntetve. A sejt-sejt kommunikáció miatt az indirekt hatások is szerepet kaphatnak és akkor a fenti görbék is módosulhatnak. Számos indirekt hatást ismerünk, például a gén instabilitás, a bystander hatás, az indukált apoptózis stb. Ezekbe most nem mennék bele, csupán annyit, hogy e hatások is modellezhetők, én példáil kifejlesztettem egy indukált apoptózis modellt.
Ha kiszámítottuk a sejtdózist, illletve annak eloszlását, akkor megbecsülhető a sejthalálban és a sejttranszformációban kifjezett biológiai hatás. A besugárzott sejt túlélési valószínüsége exponenciálisan csökken a dózissal. Ennek megfelelően, a sejthalál valószínűsége nő a kapott dózissal. Ezért, ha a dózist a modelljeinkkel jól becsöljük, akkor a sejthalál és annak térbeli és időbeli eloszlása is meghatározható. A transzformáció a rák felé vezető út egy fontos állomása. A sejt ezen állapotba jutása arányos a kapott dózissal, feltéve hogy a sejt túléli a sugárterhelést. Megjegyzem, hogy transzformáció valószínűsége sokkal kisebb, mint a sejthalálé. És akkor ennyi elmélet után lássunk egy-két eredményt. Elsőként egy sejthalál grafikont mutatok, ahol a vízszintes tengelyen a besugárzás időtartama látható, ami a dózissal arányos. Ennek függvényében, a függőleges tengelyen annak esélye szerepel, hogy a sejt elpusztul. A három görbe mutatja azt az esetet, amikor a légúti radioaktív részecske-kiülepedés homogén (zöld háromszögek), inhomogén és nincs tisztulás (kék négyzetek), illetve inhomogén és tisztulás is jelen van (piros pöttyök).
Látható, hogy a sejthalál esélye a dózissal nő, illetve az is, hogy az inhomogén kiülepedés forró területén (elágazás csúcsa, ahol sok részecske kiülepszik) a sejthalál valószínűsége erősen megnő. Ugyanezen az ábrán szépen látszik a tisztulás kárcsökkentő szerepe is.
Ha most a sejttranszformációt vesszük alapul, akkor a neki megfelelő grafikon a következő lesz:
2014. február 26., szerda
A sugárzás hatásának egy lehetséges modellezése. II. Rész: A légutakban kiülepedett radioaktív izotópok tisztulása
Miután az előző bejegyzésben a belélegzett radioaktív részecskék légzőrendszeri kiülepedését mutattam be, jelen posztot a tisztulásnak, mint védekező mechanizmusnak a részecskemennyiségre (összefüggésben áll a kapott dózissal) és eloszlásra gyakorolt hatásának szentelem.
Maga a nyák egy gél, amelynek nagy része víz, de többek között összegabalyodott polimerszálak is vannak benne, melyek többé-kevésbé egy rácsot alkotnak. Mikroszkópos felvételen ez valahogy így fest:
Látható, hogy az átlagos rácsméret néhány száz nanométer. Ennek az a következménye, hogy az ennél nagyobb részecskék elakadnak és együtt mozognak a nyákkal (nagyjából 1 mm/perc sebességgel), de a kisebb semleges részecskék szabadon diffundálnak a szálak között, akár a vízben.
A tudomány jelen állása szerint azonban nem minden részecskére hat e tisztulási forma és a részecskeméret csökkenésével előtérbe kerül a lassú tisztulás. A lenti ábra szerint, míg egy 7 mikronos részecske biztosan kitisztul a nyákkal, addig egy 1 mikron alatti csak 20-30 % eséllyel tud gyorsan (percek, órák, nap) kitisztulni. A lassú tisztulás úgy 20 napot jelent és pontos mechanizmusa nem ismert.
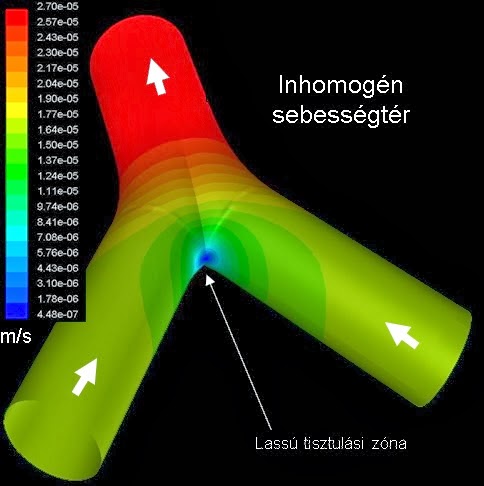
A nyáktisztulást, ugyanúgy mint a légzőrendszeri levegő- és részecskeáramlást, numerikus áramlástani eljárásokkal (CFD) lehet modellezni. A következő ábra a nyák sebességterét mutatja egy légúti elágazásban. A kék a kisebb, míg a piros szín a lokálisan nagyobb sebességet jelőli.
A légutak különböző régióiban kiülepedett részecskék káros hatása ellen a szervezet többek között úgy védekezik, hogy megpróbálja eliminálni azokat. Mivel a radioaktív részecskék miatti tüdőrák leggyakrabban a bronchiális régióban (hörgők) fordul elő, itt is az erre a régióra jellemző tisztulási mechanizmusokra szorítkozom. E régióban a legjelentősebb tisztulási formák a mukociliáris tisztulás (nyáktisztulás) és a lassú tisztulás.
A mukociliáris tisztulás a fő tisztulási mechanizmus a bronchiális légutakban a kiülepedést követő 48 órában. A légutak falán lévő csillószőrök koordinált csapkodással mozgatják a légutakat borító viszkózus nyákot, mely a garat irányába mozgatja a benne kitapadt részecskéket (onnan lenyeljük, kiköhögjük, kiköpjük). Valahogy így:
Maga a nyák egy gél, amelynek nagy része víz, de többek között összegabalyodott polimerszálak is vannak benne, melyek többé-kevésbé egy rácsot alkotnak. Mikroszkópos felvételen ez valahogy így fest:
Látható, hogy az átlagos rácsméret néhány száz nanométer. Ennek az a következménye, hogy az ennél nagyobb részecskék elakadnak és együtt mozognak a nyákkal (nagyjából 1 mm/perc sebességgel), de a kisebb semleges részecskék szabadon diffundálnak a szálak között, akár a vízben.
A tudomány jelen állása szerint azonban nem minden részecskére hat e tisztulási forma és a részecskeméret csökkenésével előtérbe kerül a lassú tisztulás. A lenti ábra szerint, míg egy 7 mikronos részecske biztosan kitisztul a nyákkal, addig egy 1 mikron alatti csak 20-30 % eséllyel tud gyorsan (percek, órák, nap) kitisztulni. A lassú tisztulás úgy 20 napot jelent és pontos mechanizmusa nem ismert.
A nyáktisztulást, ugyanúgy mint a légzőrendszeri levegő- és részecskeáramlást, numerikus áramlástani eljárásokkal (CFD) lehet modellezni. A következő ábra a nyák sebességterét mutatja egy légúti elágazásban. A kék a kisebb, míg a piros szín a lokálisan nagyobb sebességet jelőli.
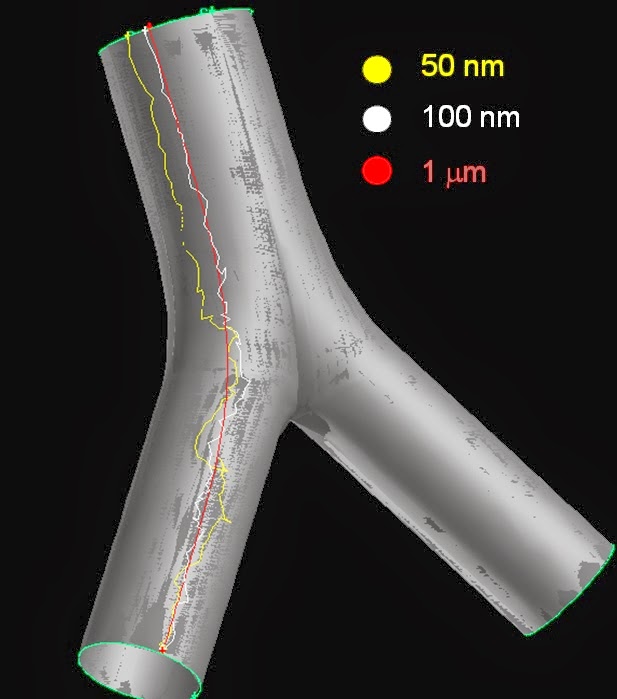
Látható, hogy amint a nyák felfele kúszik, az elágazás csúcsában lelassul. Ha visszaemlékszünk, ez volt az a hely, ahol a radioaktív részecskék a legnagyobb számban ülepedtek ki. Ha nemcsak a nyák, hanem a részecskék mozgását is modellezzük a kiülepedés után, akkor a lentiekhez hasonló pályákat kapunk:
Az ábrán láthatjuk, hogy minél kisebb egy részecske, annál többet bolyong, ami a nyák fent említett rácsos struktúrájával van összefüggésben. Mindez konkrét radonszármazékokra igy néz ki:
Azok a pályák, amelyek végigmennek az Y elágazáson, olyan részecskéknek felelnek meg, melyek a légutak mélyebb régióiból jönnek tisztulás által és átutaznak az elágazáson, míg azok amelyek végpontja az elágazásban kezdődik az oda kiülepedett részecskékhez rendelhetők. Ahol a vonalak színe megváltozik, ott bomlás történik. A bomlás helyét és a neki megfelelő energiát lejegyezzük, mert a biológiai hatás modellezésekor ebből indulunk ki. Mindezt a következő bejegyzésben fogom bemutatni.
Mindent egybevetve, a szimulációk azt mutatják, hogy a tisztulás nagymértékben csökkenti a kapott dózist és kisebb mértékben a dóziseloszlás inhomogenitását.
Hogy ezt hogyan köthetjük össze a konkrét biológiai hatással, azt a soron következő alkalommal vázolom.
2014. január 26., vasárnap
A sugárzás hatásának egy lehetséges modellezése. I. Rész: A radioaktív izotópok útja és kiülepedése a légutakban
A következőkben egy 3 részesre tervezett modellezésről szóló izelítő első részéről olvashattok/olvashatnak. Ennek során áttekintem miként modellezhető a légzőrendszerbe jutó izotópok transzportja és kiülepedése. A folytatásban a kiülepedett radioaktív részecskék tisztulásáról lesz szó, majd a harmadik részben a radioaktív részecske-sejt kölcsönhatás szimulációját mutatom be.
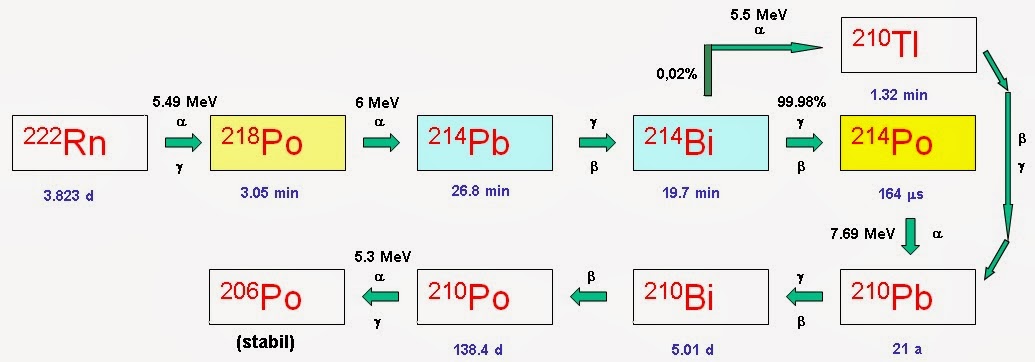
A természetes háttérsugárzásból származó radioaktív sugárterhelés több mint felét a radon leányelemeitől kapjuk. A radon gáz bomlása során 218Po keletkezik, mely alfa-aktív és nagyjából 3 perces felezési idővel 214Pb-re bomlik, majd a 214Bi-en keresztül a 214Po-hoz jutunk, ami szintén alfa-aktív. Elbomlása során 210Pb keletkezik, amely már nem rövid felezési idejű. A pontos bomlási lánc az alábbiakban látható.
A fenti radontermékek vízmolekulákkal együtt, vagy a légköri aeroszolokra tapadva vannak jelen a levegőben, ahonnan belélegezzük őket. A légzőrendszerben kitapadva elbomolhatnak és károsíthatják a sejteket/szövetet. A kár szempontjából leginkább az alfa-bomló izotópok a figyelemre méltóak (218Po, 214Po). A belélegzett izotópok légúti kiülepedését és bomlását matematikai/fizikai modellekkel tudjuk leírni. Ehhez modelleznünk kell azok pályáit, amint a levegőárammal repülnek, majd esetleg a légút falának ütköznek. A levegő és részecskeáramlást modellezhetjük idealizált, vagy CT képekből rekonstruált háromdimenziós légutakban is. Rekonstruált felső (bal oldal) és centrális (jobb oldal) légúti geometriák digitális modelljei az alábbiakban láthatók.
A levegő áramlási tere e geometriákban igen bonyolult, de a légutakban áramló levegő sebessége és nyomása numerikus áramlástani módszerrel kiszámítható. Ilyen sebességteret szemléltet az alábbi ábra. A kék jelenti a kis, a piros pedig a nagy sebesség értékeket. A számításokat a FLUENT nevű CFD (computational fluid dynamics, numerikus áramlástan) szoftverrel végeztem.
A kiszámított levegőáramlási térbe részecskéket helyezve követhető, hogy azok hol csapódnak a légutak falának. A kicsapódó részecskék beleragadnak a légutak falát borító nyákba. Az 1 és 10 mikrométeres részecskék kiülepedési mintázatát az alábbi ábrán láthatjuk nyugodt légzésnek megfelelő áramlási viszonyok (térfogatáram = 18 liter/perc) mellett. A kiülepedéseloszlás erősen inhomogén, melynek következtében egyes területek nagyobb sugárterhelést kapnak ha a kiülepedett részecskék elbomlanak.
A kiülepedett rövid felezési idejű izotópok ha elbomlanak, akkor a kiülepedés helyéhez közeli sejteket alfa-találat érheti, azokban energialeadás történik, melynek biológiai következményeit szintén lehet modellezni. De még mielőtt e fontos lépést bemutathatnám, fontos megjegyezni, hogy a fenti ábrán látahtó kiülepedési képeket módosíthatja még a mukociliáris tisztulás is, melynek modellezéséről a következő bejegyzésben lesz szó. Azt követi majd a részecske-élő anyag interakció modellezésének bemutatása.
2013. december 21., szombat
Rendhagyó bejegyzés Mexikó kapcsán
Bár közeleg az év vége, így jöhetne egy rendkívüli bejegyzés, mégsem ez szolgáltatja az apropót, hanem egy Mexikóból érkezett hír.
Röviden: Mexikó egyik városában december 2-án elloptak egy teherautót, ami radioaktív kobalt-60-as izotópot szállított. A sugárforrás egy kórházból származott, ahol azt sugárterápiás kezelések során használták. A szállítmány a lerakóba tartott, de a tudósítások szerint az autó sofőrje egy benzinkútnál pihenőt tartott. A fegyveresek itt támadtak rá és vitték el a teherautót. Valószínüleg tudomásuk sem volt a sugárforrásról. Később azt ki is dobták, de előtte még kibontották a rakományt és a védőpajzsot is.
Néhány sajtócím:
"Mind meghalnak: sugárzó
anyagot loptak el egy teherautóval"
ma.hu
"Elloptak egy
radioaktív anyagot szállító teherautót Mexikóban – jelentette a Nemzetközi
Atomenergia-ügynökség. A járművet aztán szállítmányával együtt alig két
kilométerrel arrébb megtalálták. A sugárzó anyag csomagolását a tolvajok
megbontották – a hatóságok szerint halálos dózist kaphattak"
atv.hu
„Amikor a teherautót
ellopták, az anyag megfelelő védelemmel volt ellátva. Ugyanakkor, ha
eltávolítják a pajzsokat, vagy azok megsérülnek, rendkívül veszélyesek
lehetnek”
IAEA (International Atomic Energy Agency) álláspont.
IAEA (International Atomic Energy Agency) álláspont.
Mivel ez a blog a radioaktív sugárzással és annak emberre gyakorolt hatásával foglalkozik, gondoltam kicsit számolok, hogy megtudjam tényleg kaphattak ilyen nagy dózist a tolvajok vagy sem. Az ehhez szükséges legtöbb ismeret már az előző bejegyzésekben szerepel, de akkor most újra felidézzük és alkalmazzuk azokat "élesben".
A 60Co bomlási sémája és információk a forrásról
Látható, hogy a bomlás során két különböző energiájú gamma keletkezhet. Ezek átlagenergiája 1.25 MeV. Fontos információ még, hogy 1 gr 60Co aktivitása nagyjából 44TBq (~1100 curie). [1Bq = 1 bomlás másodpercenként]. A szóban forgó forrás úgy 2500-3000 curie aktivitású volt. Ez körülbelül 110 TBq aktivitásnak felel meg.
A kapott dózis kiszámítása
Az aktivitás és a dózis között a kapcsolat nem triviális. Az elbomló atommagtól való távolság, az expozíció szöge, a lehetséges árnyékolás és természetesen az expozíció idejőtartama is befolyásolja a dózist. Ökölszabályként, 1 mSv dózist az 1 méterre lévő 60 mikrogramm 60Co okoz 1 óra alatt. Ezek alapján, ugyancsak egy óra alatt, 40 Sv dózist szenvedne el egy ember, ha a mexikói forrástól 1 méterre tartózkodna. Látható, hogy ez a halálos dózis 5-szöröse. Ha tehát valaki 12 percet tölt a forrás mellett, megkapja a halálos dózist, ha 6 percet, akkor a félhalálos dózist és így tovább. Ha valaki fogja a forrást (pl. leemeli a teherautóról), akkor a távolság 1 méternél kisebb, mondjuk a fele. Ilyen esetben a dózis nem duplája, hanem még annál is több, mert a forrás több mint kétszeres térszögben "látja" az illetőt.
Pontos információ hiányában a fenti becslések igencsak megközelítőek, de látható, hogy ezúttal a média nem biztos, hogy sokat túlozott és tényleg fennáll a veszélye, hogy életveszélyes dózist szenvedtek el a tolvajok.
Megjegyzés1: A fenti dózisok egésztest dózisok. Lokálisan ennél sokkal nagyobb dózist is kaphattak. Az elnyelt dózist úgy kapjuk, hogy az elnyelt energiát elosszuk a tömeggel. Látható, hogy mondjuk ha megfogták a forrást, akkor a kézdózis a fentieknek sokszorosa lehet, mivel annak tömege kicsi az egész testhez képest, ráadásul a forrás nagyon közel van a kézhez.
Megjegyzés2: A mai számítógépek lehetőséget nyújtanak arra, hogy sokkal pontosabban és elegánsabban számítsunk dózist. Persze az expozíció körülményeire így is szükség van. Ha valaki ügyes, írhat egy programot és kiszámolhatja, hogy a teljes térszögből a forrás körül mennyi jut az emberre, mennyi energiát nyel el a levegő és mennyit az ember, mindezt akár 3D-ben.
http://en.wikipedia.org/wiki/Cobalt-60
http://index.hu/tudomany/2013/12/05/ezert_ne_lopj_radioaktiv_izotopot/
http://www.popularmechanics.com/science/energy/nuclear/mexican-truck-thieves-and-cobalt-60-explained-16236157
http://en.wikipedia.org/wiki/Curie
----------------------------------------------------------
VÉGEZETÜL, MINDEN KEDVES OLVASÓMNAK KÍVÁNOK SIKERES, BOLDOG ÚJ ÉVET!

2013. november 30., szombat
A sugárzások biológiai hatásának vizsgálati módszerei
A mai bejegyzésben a sugárzások hatásának leggyakoribb vizsgálati módszereit veszem számba, röviden ismertetve azokat, majd megemlítve ezek néhány előnyét és hátrányát. E módszerek az in vivo és in vitro besugárzások, az epidemiológia és a modellezés. E módszerek egymásnak nemcsak konkurensei, de kiegészítői is.
Emberi besugárzások
Induljunk ki abból az alapvető etikai szabályból, hogy szándékosan, kutatási vagy egyéb célból, embereket besugározni tilos.Ettől még persze mindenkit ér sugárzás, ha nem más, akkor a természetes háttérsugárzás. De ezen kívül, az orvosi diagnosztika egyre több olyan módszert, eszközt használ, melyek révén növekszik a sugárterhelés, főleg a fejlett országokban. Itt most csak egyet említenék, a CT-t (computer tomography), ami egy egyre elterjedtebb orvosi képalkotó technika és eszköz. Egy átlagos mellkas CT során úgy 7 mSv, egy koponya CT alkalmával pedig megközelítőleg 2 mSv effektív dózist (korábbi bejegyzésben definiáltam) kapunk. Emlékeztetőül, átlagosan egy ember a háttérsugárzásból egy év alatt 2,5 mSv effektív dózist kap. Ennél sokkal nagyobb dózisokat kapnak a betegek a sugárterápia során.
Egy másik lehetséges sugárterhelés, ami a sugárbalesetek során ért embereket. E balesetek egy csokorba szedve, igényesen bemutatva magyarul is megjelentek Somlai János Esetek-sugárbalesetek című könyvében
http://www.libri.hu/konyv/esetek-sugarbalesetek.html
Mindezen sugárterhelések hatását tanulmányozni lehet és tanulmányozza is a szakma.
Állatkísérletek
Ha már tilos embereken kísérletezni, akkor első megközelítésben kézenfekvő lenne az ismert biológiai rendszerek közül az emberhez felépítésében és működésében leginkább hasonlító
állatokat besugarazni, majd vizsgálgatni. Azonban az álatkísérleteket szabályozó rendelkezések az idő teltével egyre szigorodnak. A legtöbb besugárzásos kíséreletet patkányokon és egereken végzik. Az eredmények értékelésekor mindíg fennállnak az állatról emberre történő extrapolálás nehézségei (különböző komplexitás, különböző radioszenzitivitás stb).
Epidemiológia
Az epidemiológia eredetileg járványok terjedésével foglalkozott, de mára jelentése kiszélesedett. Ma egy adott, jól definiált populációban valamilyen betegség vagy egészségügyi állapot eloszlásának, okának, következményeinek vizsgálatát jelenti. A sugárepidemiológia természetesen a sugárzásnak kitett populációval foglalkozik. Tipikus példája, amikor egy populációban a dózis és az egészségügyi hatás közötti összefüggést vizsgáljuk, mint például a Japánra ledobott atombombák túlélőinél a leukémia vagy tüdőrák előfordulási gyakoriságának a vizsgálata, de az uránbányászokat, sőt az átlagpopulációt is sokat vizsgálják.
Sejtbesugárzási
kísérletek
A sugárbiológia egyik leggyakoribb módszere, hogy tenyésztett sejtvonalakat tezsnek ki különböző típusú és erősségű sugárzásnak, majd követik annak hatását, valamilyen jól definiált biológiai végpontra (sejthalál, mutáció stb.). Ezen kísérletek ellenőrzött körülmények között történnek, így bizonyos paraméterek hatása kizárható, másoké jól vizsgálható. Sajnos egy ilyen in vitro rendszer sok tekintetben másképp viselkedik, mint a szövetbe, szervekbe, szervezetbe rendezett sejtek.
Modellezés
A számítógép kapacitások folyamatos növekedése és a numerikus eljárások fejlődése és novekvő hozzáférhetősége kedvez a számítógépes modellezés elterjedésének. Így van ez a sugárbiológia területén futtatott szimulációkkal is. Ezen módszerek viszonylag olcsók, reprodukálhatók és számos olyan paraméter módosítható tetszőlegesen, ami a gyakorlatban nem, vagy csak nehezen lenne megvalósítható. A modellezés eredményére viszont mindíg szkeptikusan kell tekintenünk és ahol lehet, a modellt validálnunk kell az elérhető kísérleti eredményekkel.A modellezésről még sok szó fog esni, mivel jómagam is elsősorban e területen vagyok érdekelt, de végezetül még vázlatosan összeírtam a fenti módszerek néhány előnyét és hátrányát.
Emberi besugárzások
Előny
- valós emberi szervezettel van dolgunk, így az eredmény a leghitelesebb/relevánsabb.
- etikai korlátok
Előny
- nem kell embereket sugarazni
- általában tilos (egér, patkány a leggyakoribb)
- állat-ember extrapollálás (különböző radioszenzitivitás) nehézségei
Előnyök
- valós embereken valós hatásokat vizsgál, anélkül, hogy besugaraznánk
- kis dózisokra szór (rossz statisztika)
- populációra vonatkozik, nem adott egyénre
- nem ad információt a mechanizmus(ok)ról
Előnyök
- ellenőrzött körülmények
- bizonyos paraméterek rögzíthetők
- jól tanulmányozhatók a mechanizmusok
- drágák (modellezéshez képest)
- in vitro-in vivo extrapolálási dilemmák
- idealizált rendszer és körülmények
Előnyök
- olcsó
- könnyű a paraméterekkel manipulálni
- reprodukálható
- akárhányszor megismételhető, módosítható
- bármikor továbbfejleszthető
- olyan tartományolban is működik, ami a kísérletekkel nem megvalósítható
- egyszerűsített valóság
- az eredmények sokszor nehezen ellenőrízhetők
- a modellparaméterek valós értékeit sok esetben nem ismerjük
2013. október 3., csütörtök
Egy kis segédanyag a sugárzás utáni események jobb megértéséhez
Mivel a legutóbbi bejegyzés (Mi
történik a besugárzott élő szervezetben?) a szokásosnál egy picit hosszabb és
töményebb volt, gondoltam relaxálásul ajánlok néhány multimédia anyagot az ott
leírtakkal kapcsolatosan. Van köztük egészen elemi, de tudományosabb is. Csak
egy csipetnyi abból, amit a világhálón találhatunk a témában. Aki kitartóan keres könnyen találhat hasonló, vagy még ennél is relevánsabb anyagokat.
Élvezzék/élvezzétek!
Kezdetnek egy kis “laza” 3D animáció
Szabad gyökök elemi bemutatása
A víz besugárzása (prezentáció, tudományosabb)
Mutációk keletkezése
DNS sérülés és kijavítás
Feliratkozás:
Bejegyzések (Atom)